ժҪ:���йػ�����רҵ���ң�
|
���йػ�����רҵ���ң�



��һ����רҵ�����о��ߡ��о���ʿ��ҩ�����Ա�� ����������ίԱ�����Σ������Σ���ίԱ�����鼰�����Ա�� �������������Σ���ֹ�Ժ���������������Ρ����������鼰��Ŀ������Ա�� ���ģ���췽��CRO��˾�Լ�SMO��˾����ش�ҵ��Ա�� 

2020��8��7-8�� 

��ҽ��Ժ21¥��һ������ Ժ����Ա���ϲλ� ���������ͻ������ӣ� 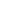


���λ��齫��������������ѧ��Ȩ����֪�����ڼ����зḻʵ��������������������ר���ڿβ����ɡ� 

������ѵ�ɽ���ʡҩѧ��ҩ���ٴ������о�רҵίԱ��ί������ҽ�ƴ�ѧ����ҽԺ����а졣 

�����ѵ��λ��2020��08��06��ǰ���λ���Ա��Ϣ������ ���䣺xyfy2369@163.com ��ϵ�绰��0516-85802369 ��ϵ�ˣ������� 15862143768 
����鿴��ͼ 
ҩ���� ������˹��ҽҩ�Ƽ�����˾ ����Խ��ʹҽҩ�Ƽ���չ����˾ ����˼Ĭҽҩ�Ƽ�����˾ �Ͼ���˳����ҽҩ����˾ �Ͼ���ķŷҽҩ�Ƽ�����˾ ����˹���Ϻ���ҽҩ�Ƽ������ɷ�������˾ �Ϻ���ʯҽҩ�Ƽ�����˾ �Ϻ��к�ҽҩ�Ƽ�����˾ ��˹���ǣ�������ҽҩ�����о��������ι�˾ �Ŵ�������ҩ(���ݣ�����˾ ʯҩ��������˾ ������Դ���ҽҩ�Ƽ�����˾ �Ϻ���������ҽҩ�Ƽ�����˾ ��˼��ҽҩ���Źɷ�����˾ �����Ȼ�ҽҩ�Ƽ�����˾ �������������Ⱥ� |
- ��һƪ����TQM��ȫ�������������������
- ��һƪ��û����












̸̸���Ը����µĿ�