ժҪ:����·���ɫ�����˽����·���ѵ���ݣ��� 8��21�պ���-2020�걨��������Ҫ�Ϲ������дʵս 9��4���Ϻ�-�ڶ��ڡ�2020�з���QCʵ���ҺϹ����ר���� 9��11������-2020ҩƷ���ݹ����淶ʵʩ���� 9��25�ռ���-���Ӧ�Բ���Ч����ʵ����OOS�ķ���ר����ѵ 8
|
����·���ɫ�����˽����·���ѵ���ݣ��� 8��21������-2020�걨��������Ҫ�Ϲ������дʵս 9��4���Ϻ�-��������2020�з���QCʵ���ҺϹ����ר���� 9��11������-2020ҩƷ���ݹ����淶ʵʩ���� 9��25�ռ���-���Ӧ�Բ���Ч����ʵ����OOS�ķ���ר����ѵ 8��27�ճɶ�-�ڶ��ڡ�ҩƷ�з�����������ϵ������ʵʩ��ά�������������ٵ�������Բߡ� �μ���ѵ�ɻ��ֵ499Ԫҩ�ɲ�������ѵ��Ȼ�Ա����ѯ�������������ϵ�����-13120221304���š�
9��11�պ���-ͳ�Ƽ���������GMPʵʩ��Ӧ��ʵ����ѵ 8��20���Ͼ�-2020��ҩ����ҵʵʩӦ��ר�����ְ� 8��12���Ϻ�-����FDA��ŷ��GMP������ϵ���ֳ�GMP������Ʒ�����ȱ�ݼ��ظ���ʽ����� 9��9�պ���-�ڶ��ڡ�2020��������ҵMAH�ۺϹܿ���ϵ����ʵս�� 8��21���Ͼ�-2020 MAH�ƶ�ȫ��ʵʩ����ҵӦ�Բ��� 9��3���Ϻ�2020ȫ��ҩ����ҩ��ˮ���涯̬��ȫ������������ 8��21���Ϻ�-ҽҩ�������������Զ�����ȫ��������Ƹ���ѵ
ת�ԣ�ҩ��֮�� 2020�з���QCʵ���ҺϹ����ר����ѵ ���йص�λ�� 2020��ͻ�����������飬����������ҩ��ҵ�����˾��Ӱ�졣��һ���棬ҩ������һϵ���ļ���������ҩ������ע������취���Լ������ල�����취�ȣ�Ҳ��������ҩ��ҵ���ճ��ϸ���������˸����ѹ���� һֱ��������ҩ��ҵ���з���GMPQCʵ���Ҷ��Ǿ�����������İ�飬������FDA ��483�۲��Խ��Խ���ʵ���ҹ������⡣�ճ���Ӫ���������������������豸��֤��������Ա�ĺϹ����������ͬʵ����������ϵ�����ܲ��ɷֵģ�һ�����õ�����������ϵ���ܹ���֤ʵ���ҵ����еĹ����кϹ桢�Ϸ����������ϸ�ķ��л��걨���ݡ� ���ǣ��ն��ķ������ģ���������ʵ�����ճ���ӪSMP��SOP�У�����Ȼ�Ǵ�ҹ��ļ����ɻ�����⡣����ܹ���ʵ��Ϊ�����������µķ��������������з���cGMP QCʵ����������ϵ�У���ͬ�ֳ��˲��л���ϣ����ո�������������������ڸ�ҩ������������Ч�ʡ����㷨������ԣ����ǽ�Լ�ճ���Ӫ�ɱ�����������dz���İ�������Щ���ݣ����۶�������������Ա������������Ա����֤������Ա�ȶ���ʮ�ָ���Ȥ����ġ� Ϊ�ˣ�����λ����2020��9�� 4����6�����Ϻ��оٰ�ڶ��ڡ�2020�з���QCʵ���ҺϹ����ר����ѵ�ࡱ������ҵ��Ȩ��ר��������������������������ѵ֪ͨ������ һ�����鰲�� ����ص㣺�Ϻ��У�����ص�֪ͨ���ѱ�����Ա�� ����ʱ�䣺2020�� 9��4��- 9�� 6��( 4��ȫ�챨��)
����������Ҫ�������ݼ�������ʦ �����������һ���γ̰��ű���
�����λ���� �з�����ҩ��˾���з���QA��QC����ز�����Ա��
�ġ�����˵�� 1�����۽���,ʵ������,ר�⽲��,�������� 2�������α���Ϊ��ҵ������ר�ң���ӭ������ѯ 3�����ȫ����ѵ�γ�����Э��䷢��ѵ֤��
�塢������� 1.����ѣ�2500Ԫ/�ˣ�����Ѱ�������ѵ�����֡���������Ъ�ȣ���ʳ��ͳһ���ţ����������� 2.�μ���ѵ��ѧԱ����ü�ֵ499Ԫҩ�ɲ�������ѵƽ̨��https://appnv8mypmx8987.h5.xiaoeknow.com/homepage����Ȼ�Ա�������ٽ�ϵͳ�γ����ѧϰ�� ����ҩ�ɲ�רҵҽҩֱ����ѵ 1��ҩ�ɲ�VIP��Աһ��499Ԫ /�꣬�Ź���360Ԫ /�� 2����ҵVIP�Ź���ļ�У�8000Ԫ /�� 3���γ����鼰����������ѯ��������ϵ��
�ߡ���ϵ��ʽ ����ϵ�ˣ��� �� Q Q��525182570 �� ��:13120221304 �� �䣺13120221304@163.com ����һ�������ճ̰��� ���������λᱨ����
�������������� ����һ���� �� �� �� ��
���������ڶ���2020�з���QCʵ���ҺϹ����ר����ѵ��--��ִ�� ���λ�������������������
����·���ɫ��������˽������ѵ���� ���£����·ݸ�������ҩ�������� ����·����Ķ�ԭ�ġ���������ֱ����������� ע��������ת����������Ȧ�����������ҩѧ�����Ⱥ��������13120221304������ͼ����ѡ����ȡ���༭���в���ҽҩ�����μ��� |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




























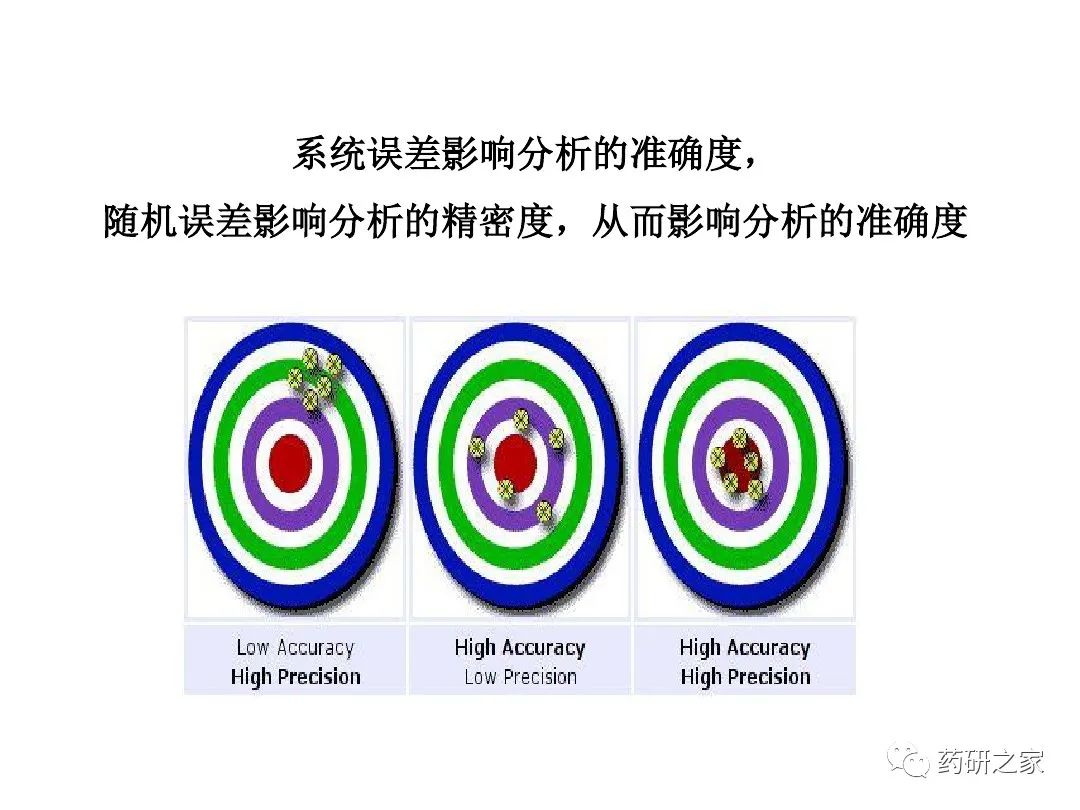

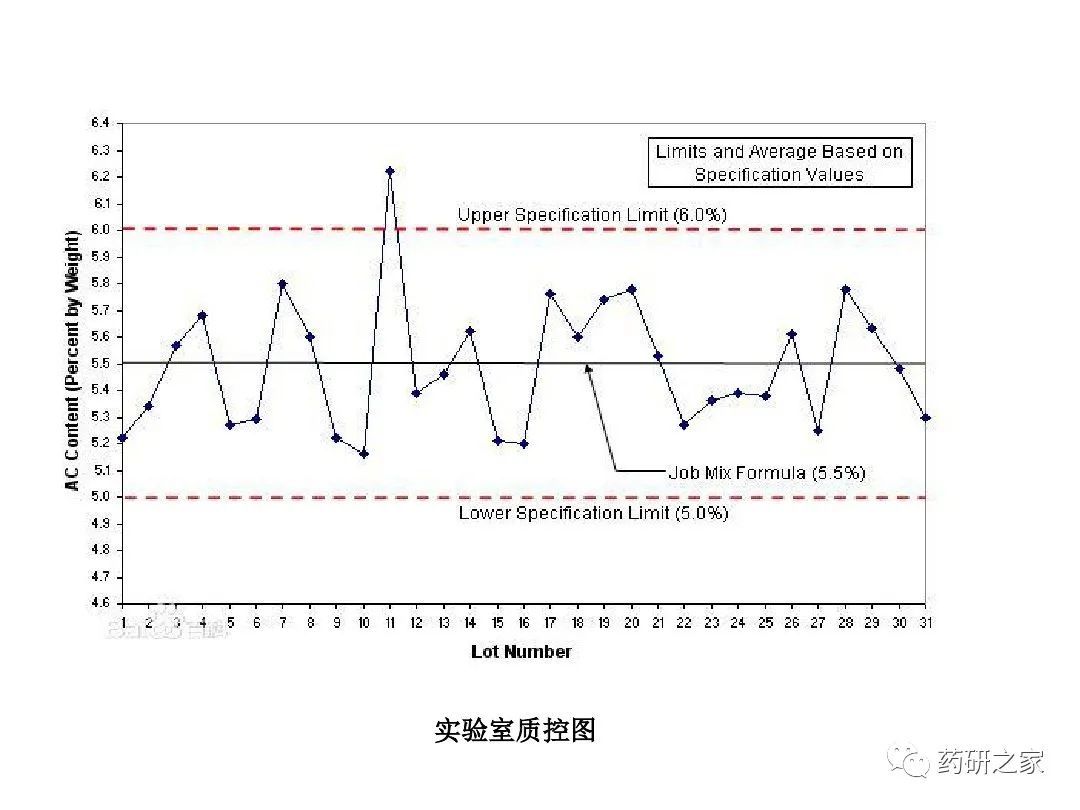

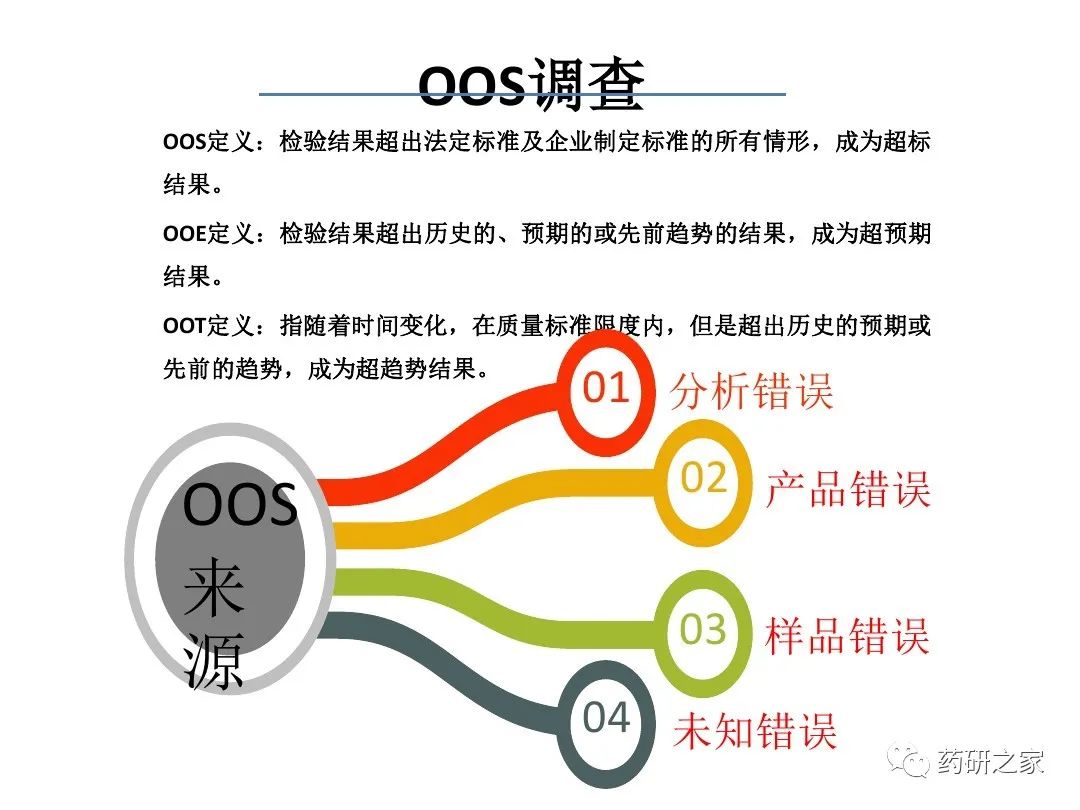



̸̸���Ը����µĿ�